Diferencia entre revisiones de «Ecuación de Nernst»
mSin resumen de edición |
mSin resumen de edición |
||
| Línea 1: | Línea 1: | ||
Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso <code>Ox<sub>1</sub></code> oxida a <code>Red<sub>2</sub></code> ya que <code>Ox<sub>2</sub></code> no puede oxidar a <code>Red<sub>1</sub></code>; se dice entonces que <code>Ox<sub>1</sub></code> es un oxidante más fuerte que <code>Ox<sub>2</sub></code> al mismo tiempo que <code>Red<sub>2</sub></code> es un reductor más fuerte que <code>Red<sub>1</sub></code><ref name=":0">Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.</ref>. | Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso <code>Ox<sub>1</sub></code> oxida a <code>Red<sub>2</sub></code> ya que <code>Ox<sub>2</sub></code> no puede oxidar a <code>Red<sub>1</sub></code>; se dice entonces que <code>Ox<sub>1</sub></code> es un oxidante más fuerte que <code>Ox<sub>2</sub></code> al mismo tiempo que <code>Red<sub>2</sub></code> es un reductor más fuerte que <code>Red<sub>1</sub></code><ref name=":0">Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.</ref>. | ||
Para realizar tales predicciones de manera cuantitativa medimos el '''<u>potencial estándar de reducción (< | Para realizar tales predicciones de manera cuantitativa medimos el '''<u>potencial estándar de reducción (<code>E°</code>)</u>''' (REVISAAAAAR!!!!!!) para lo cual suponemos un sistema de dos semirreacciones (una de ellas estándar de valor 0 ''V'' y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la '''Ecuación de Nernst''' cuya forma es: | ||
[[Archivo:Ecuación de Nernst completa.png|centro|sinmarco|275x275px]] | [[Archivo:Ecuación de Nernst completa.png|centro|sinmarco|275x275px]] | ||
Donde | Donde | ||
Revisión del 13:55 16 ene 2026
Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso Ox1 oxida a Red2 ya que Ox2 no puede oxidar a Red1; se dice entonces que Ox1 es un oxidante más fuerte que Ox2 al mismo tiempo que Red2 es un reductor más fuerte que Red1[1].
Para realizar tales predicciones de manera cuantitativa medimos el potencial estándar de reducción (E°) (REVISAAAAAR!!!!!!) para lo cual suponemos un sistema de dos semirreacciones (una de ellas estándar de valor 0 V y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la Ecuación de Nernst cuya forma es:
Donde
- se refiere al potencial estándar de reducción
- se refiere a la constante de los gases ideales
- se refiere a la temperatura absoluta del sistema
- se refiere a la mol de electrones intercambiados por semirreacción
- se refiere a la constante de Faraday Si la
- y refieren a la concentración molar de cada especie oxidante y reductora
Si trabajamos en condiciones normales de temperatura () y transformando el logaritmo natural a uno base diez podemos aproximar la ecuación de Nernst a la siguiente:
Siguiente página: Cálculo del potencial en el Punto de Equivalencia (PE)
- ↑ Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.
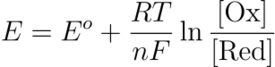

![{\textstyle [{\text{V}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9c3912f87121e1646a40af1463079ff9e993b043)

![{\textstyle [8.31446{\frac {J}{mol*K}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3b3cf04ba4f3f404a674b94aee9f4aaef8f46e0f)

![{\textstyle [{\text{K}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/073afa5e761760165200fa4c32392be797dfacf6)

![{\textstyle [{\text{mol}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/de439418b78ecbedca792f5859d229fb89d315e8)

![{\textstyle [eN_{A}=96485.33212{\frac {C}{mol}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/afe62deddb1d647d5daabdc4ce352cd94a6dae8d)
![{\textstyle [{\text{Ox}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/618c707f00f92072e2675c212003a973b3ff129e)
![{\textstyle [{\text{Red}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f1581fe41277114db8800aa61b85b68eefc48cc9)
![{\textstyle [{\frac {mol}{L}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a3ef4ff305f78092303a4cc98f6511db1185e5c3)

![{\displaystyle E=E^{o}+{\frac {0.058}{n}}\log _{10}{\frac {\text{[Ox]}}{\text{[Red]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5a2ff06a0650d5e373d30c360627d3baef92bb26)