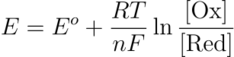Diferencia entre revisiones de «Ecuación de Nernst»
mSin resumen de edición |
mSin resumen de edición |
||
| Línea 1: | Línea 1: | ||
Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso <code>Ox<sub>1</sub></code> oxida a <code>Red<sub>2</sub></code> ya que <code>Ox<sub>2</sub></code> no puede oxidar a <code>Red<sub>1</sub></code>; se dice entonces que <code>Ox<sub>1</sub></code> es un oxidante más fuerte que <code>Ox<sub>2</sub></code> al mismo tiempo que <code>Red<sub>2</sub></code> es un reductor más fuerte que <code>Red<sub>1</sub></code><ref name=":0">Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.</ref>. | Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso <code>Ox<sub>1</sub></code> oxida a <code>Red<sub>2</sub></code> ya que <code>Ox<sub>2</sub></code> no puede oxidar a <code>Red<sub>1</sub></code>; se dice entonces que <code>Ox<sub>1</sub></code> es un oxidante más fuerte que <code>Ox<sub>2</sub></code> al mismo tiempo que <code>Red<sub>2</sub></code> es un reductor más fuerte que <code>Red<sub>1</sub></code><ref name=":0">Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.</ref>. | ||
Para realizar tales predicciones de manera cuantitativa medimos el '''<u>potencial estándar de reducción (<code>E°</code>)</u>''' (REVISAAAAAR!!!!!!) para lo cual suponemos un sistema de dos semirreacciones (una de ellas estándar de valor 0 ''V'' y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la '''Ecuación de Nernst''' cuya forma es: | Para realizar tales predicciones de manera cuantitativa medimos el '''<u>potencial estándar de reducción (<code>E°</code>)</u>''' (REVISAAAAAR!!!!!!) para lo cual suponemos un sistema de dos semirreacciones (una de ellas estándar de valor 0 ''V'' y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la '''Ecuación de Nernst completa''' cuya forma es: | ||
[[Archivo:Ecuación de Nernst completa.png|centro|sinmarco| | [[Archivo:Ecuación de Nernst completa.png|centro|sinmarco|234x234px]] | ||
Donde | Donde | ||
*< | *<code>E°</code> se refiere al potencial estándar de reducción <code>[V] = Volts</code> | ||
*< | *<code>R</code> se refiere a la constante de los gases ideales <code>[8.31446 J/mol*K]</code> | ||
*< | *<code>T</code> se refiere a la temperatura absoluta del sistema <code>[K] = Kelvin</code> | ||
*< | *<code>n</code> se refiere a la mol de electrones intercambiados por semirreacción <code>[mol]</code> | ||
*< | *<code>F</code> se refiere a la constante de Faraday <code>[e*N<sub>A</sub>=96485.33212 C/mol]</code> | ||
*< | *<code>[Ox]</code> y <code>[Red]</code> refieren a la concentración molar de cada especie oxidante y reductora <code>[mol/L]</code> | ||
Si trabajamos en condiciones normales de temperatura ( | Si trabajamos en condiciones normales de temperatura (20 °C) y transformando el logaritmo natural a uno base diez podemos aproximar a la '''ecuación de Nernst simplificada''': | ||
[[Archivo:Ecuación de Nernst simplificada.png|centro|sinmarco|231x231px]] | |||
El valor constante de <math>0.058</math> suele redondearse a <math>0.06</math> según cuanta precisión se desee. En caso de que el sistema esté representado por | |||
[[Archivo:SemiRedox completa.png|centro|sinmarco|160x160px|SemiRedox completa]] | |||
Entonces la ecuación se adapta como: | |||
[[Archivo:EcNernst3.png|centro|sinmarco|232x232px|EcNernst3]] | |||
Cabe recalcar que esta ecuación se aplica sólo a semirreacciones y no así para sistemas completos. | |||
Siguiente página: [[Cálculo del potencial de reducción para un sistema en el Punto de Equivalencia (PE)|Cálculo del potencial en el Punto de Equivalencia (PE)]] | Siguiente página: [[Cálculo del potencial de reducción para un sistema en el Punto de Equivalencia (PE)|Cálculo del potencial en el Punto de Equivalencia (PE)]] | ||
Revisión del 14:07 16 ene 2026
Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso Ox1 oxida a Red2 ya que Ox2 no puede oxidar a Red1; se dice entonces que Ox1 es un oxidante más fuerte que Ox2 al mismo tiempo que Red2 es un reductor más fuerte que Red1[1].
Para realizar tales predicciones de manera cuantitativa medimos el potencial estándar de reducción (E°) (REVISAAAAAR!!!!!!) para lo cual suponemos un sistema de dos semirreacciones (una de ellas estándar de valor 0 V y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la Ecuación de Nernst completa cuya forma es:
Donde
E°se refiere al potencial estándar de reducción[V] = VoltsRse refiere a la constante de los gases ideales[8.31446 J/mol*K]Tse refiere a la temperatura absoluta del sistema[K] = Kelvinnse refiere a la mol de electrones intercambiados por semirreacción[mol]Fse refiere a la constante de Faraday[e*NA=96485.33212 C/mol][Ox]y[Red]refieren a la concentración molar de cada especie oxidante y reductora[mol/L]
Si trabajamos en condiciones normales de temperatura (20 °C) y transformando el logaritmo natural a uno base diez podemos aproximar a la ecuación de Nernst simplificada:
El valor constante de suele redondearse a según cuanta precisión se desee. En caso de que el sistema esté representado por
Entonces la ecuación se adapta como:
Cabe recalcar que esta ecuación se aplica sólo a semirreacciones y no así para sistemas completos.
Siguiente página: Cálculo del potencial en el Punto de Equivalencia (PE)
- ↑ Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.