Métodos para Interpretar Curvas de Titulación
Introducción: El Lenguaje Gráfico
Las curvas de titulación son representaciones gráficas que permiten visualizar de manera continua cómo progresa una reacción de valoración a medida que se añade el titulante. Además de esto una curva de titulación sintetiza información química esencial sobre el sistema en estudio, como los equilibrios que predominan, la estequiometría de la reacción y las condiciones bajo las cuales puede detectarse un punto final de forma confiable.
¿Qué representa una curva de titulación?
Una curva de titulación es una representación gráfica que muestra cómo varía una propiedad química relacionada con la concentración de una especie en solución conforme se añade un volumen conocido de titulante. De manera general, el volumen del titulante agregado se representa en el eje horizontal, mientras que en el eje vertical se grafica una variable que depende directamente de la concentración del analito o del reactivo. La construcción de una curva de titulación permite describir el comportamiento químico del sistema a lo largo de toda la reacción, desde el estado inicial, hasta las condiciones posteriores al punto de equivalencia, donde el titulante se encuentra en exceso.
Elementos clave en la gráfica: punto de equivalencia, regiones y ejes
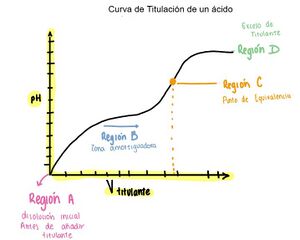
Una curva de titulación contiene varios elementos fundamentales que permiten su correcta interpretación. Uno de los más importantes es el punto de equivalencia, este corresponde al momento en que las cantidades del analito y del titulante han reaccionado de acuerdo con la estequiometría de la reacción. En la gráfica, este punto suele manifestarse como un cambio brusco en la pendiente de la curva y marca la transformación completa del analito.
Es importante distinguir el punto de equivalencia del punto final, que corresponde a un cambio físico observable, como un viraje de color de un indicador o una variación detectable en el potencial de un electrodo.
Otro elemento esencial de la curva es su división en regiones, las cuales reflejan distintos estados químicos del sistema. Cada región está dominada por especies y equilibrios diferentes, esto hace que haya cambios característicos en la forma de la gráfica.
Típicamente se distinguen:
- Punto inicial: Donde sólo está presente el analito.
- Región antes del PE: Donde coexisten el analito sin reaccionar y el producto de la reacción, formando a menudo un sistema amortiguador.
- Zona del PE: El salto brusco donde ocurre la transición.
- Región después del PE: Donde domina el exceso del titulante agregado.
Por último, la información proporcionada por los ejes de la gráfica es crucial para la interpretación. El eje horizontal representa el volumen de titulante agregado, mientras que el eje vertical muestra una propiedad relacionada con la concentración, como el pH, el pM o el potencial eléctrico. La elección de esta variable determina el tipo de información que puede extraerse de la curva y condiciona la forma en que se analizan los resultados de la titulación.
Método 1: Tabla de Variación de Composición
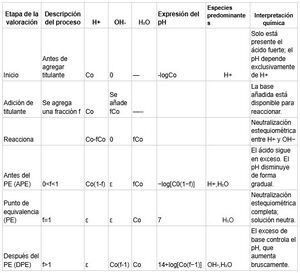
El método de la tabla de variación de composición, también conocido como método por regiones, permite desglosar el proceso de titulación en etapas bien definidas, cada una dominada por un equilibrio químico distinto.
Este método constituye una herramienta de interpretación. Al dividir la curva en regiones, se identifica qué especies químicas son mayoritarias, qué reacciones gobiernan el sistema y por qué la curva adquiere una forma específica. A partir de ella se seleccionan puntos clave que, al graficarse, generan la curva de titulación y permiten interpretar visualmente el comportamiento del sistema.
Procedimiento general
Paso 1: Definir el sistema químico de forma general (HA o H₂A y base fuerte) y su reacción.
Paso 2: Crear la Tabla de Variación: Una tabla con las columnas adecuadas para seguir cómo cambian las cantidades de reactivos y productos en cada etapa.
Cada fila de la tabla no representa únicamente un punto de cálculo, sino una situación química distinta del sistema. El análisis de la tabla permite anticipar la forma de la curva incluso antes de realizar la gráfica.
Reacción: H⁺ + OH⁻ ⇌ H₂O
| Símbolo | Significado | Descripción |
|---|---|---|
| C0 | Concentración inicial del analito | Concentración molar del analito antes de comenzar la titulación. |
| v0 | Volumen inicial del analito | Volumen (generalmente en mL o L) de la disolución de analito. |
| C | Concentración del titulante | Concentración molar del reactivo titulante. |
| V | Volumen agregado | Volumen de titulante añadido en un momento dado de la titulación. |
| VPE | Volumen en el punto de equivalencia | Se obtiene por estequiometría: C0V0 = CVPE Es el volumen donde se neutraliza exactamente todo el ácido. |
| f | Fracción de titulación | Definición: f = V/VPE Interpretación: |
| ε | Cantidad muy pequeña (no cero) | Representa una concentración residual despreciable pero no nula. Existe porque las reacciones nunca son "perfectamente completas" en el equilibrio. |
¿Qué significan las operaciones en la tabla?
- C₀(1−f)
Esta expresión aparece antes del punto de equivalencia.
¿De dónde sale?
Inicialmente hay C₀ de ácido.
Una fracción f ya reaccionó con la base.
Lo que queda sin reaccionar es: C₀ − fC₀ = C₀(1−f)
- C₀(f−1)
Esta expresión aparece después del punto de equivalencia.
¿De dónde sale?
En el PE ya reaccionó todo el ácido.
El volumen extra corresponde a base en exceso.
La cantidad sobrante es: fC₀ − C₀ = C₀(f−1)
Interpretación desde la tabla:
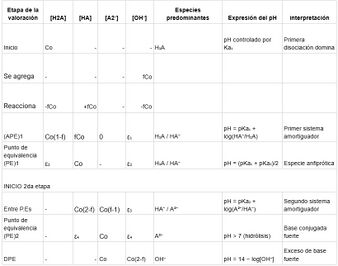
| Región | Condición | Especies predominantes | Interpretación química |
|---|---|---|---|
| A | Inicio | HA | El ácido débil controla el pH |
| B | Antes del PE | HA / A⁻ | Sistema amortiguador |
| C | PE | A⁻ | Hidrólisis de la base conjugada |
| D | Exceso | OH⁻ | El titulante domina |
Construcción y uso de la tabla de variación de composición
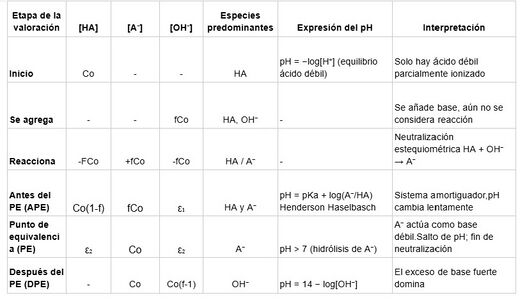
La tabla de variación de composición se construye identificando regiones de la titulación en función del volumen de titulante añadido. En cada región se analizan las especies presentes y se establecen suposiciones químicas razonables que simplifican el cálculo del pH.
1. Dividir la Titulación en Regiones Clave: Identificar la química dominante en la curva.
2. Calcular el pH en cada región: Usar la fórmula simplificada correcta, que se deduce de las especies mayoritarias en tu tabla.
3. Gráfica e interpretación: Unir los puntos calculados para ver la curva y relacionar su forma con lo visto en la tabla.
¿Cómo se grafica la curva?
Una vez calculados los valores de pH para distintos volúmenes de titulante y trazada la curva de titulación (pH vs volumen agregado), la gráfica puede dividirse en regiones bien definidas, cada una asociada a una fila de la tabla de variación de composición y a una especie química dominante.
Ejemplo: CASO 1: Ácido monoprótico débil (HA) + Base fuerte
Para este caso:
- Analito: 25.0 mL de un ácido monoprótico débil genérico HA, a una concentración de 0.10 M y con un pKa = 4.75.
- Titulante: Una base fuerte genérica (OH⁻) a 0.10 M.
Reacción principal: HA + OH⁻ → A⁻ + H2O
La tabla anterior no es el resultado final, sino una herramienta de cálculo.
Cada fila de la tabla corresponde a una región específica de la curva de titulación, y de cada región se obtiene una expresión distinta para el pH.
¿Qué se grafica?
Para visualizar la información de la Tabla de Variación de Composición, construimos una gráfica de dos dimensiones:
- Eje X (Horizontal): Representa el progreso de la titulación. Expresada como el Volumen de titulante añadido (en mL).
- Eje Y (Vertical): Representa la respuesta del sistema, que es el pH calculado para cada punto del eje X. Estos valores de pH son los resultados directos de aplicar las fórmulas simplificadas de cada región en nuestra Tabla de Variación.
¿Cómo se Dibuja la Curva a Partir de Estos Puntos?
1. Ubicar puntos en el plano: En un papel milimetrico o de manera esquemática, se ubican con precisión los puntos de la tabla anterior en el plano (Volumen, pH). 2. Unir con una línea suave (no recta): La química de una titulación es un proceso continuo. Por lo tanto, no se unen los puntos con segmentos de recta. En su lugar, se traza una curva suave y continua que pase naturalmente por todos ellos.
Esto refleja que:
- Al inicio, el pH sube lentamente.
- Alrededor del punto medio, la curva es casi plana.
- Alrededor del P.E., la curva tiene una pendiente muy pronunciada (un "salto").
- Después del P.E., la pendiente vuelve a suavizarse.
Regiones de la Curva de Titulación
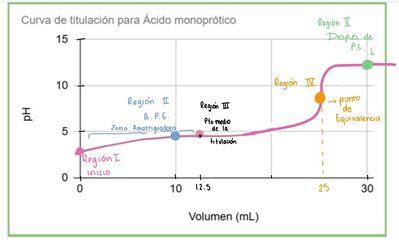
Región I: Inicio de la titulación (0 mL de titulante)
Esta región corresponde al punto inicial de la curva, caracterizado por un pH ácido moderado. Solo está presente el ácido débil. El pH inicial no es extremadamente bajo porque el ácido no está completamente disociado, lo cual se refleja en la pendiente suave de la curva en esta zona.
Región II: Zona amortiguadora (antes del punto de equivalencia)
Esta región aparece como un tramo casi horizontal de la curva. La solución actúa como un sistema amortiguador, ya que contiene cantidades comparables de ácido débil y su base conjugada. Cada adición de base provoca principalmente la conversión de ácido en su base conjugada, sin un cambio brusco de pH. Esto explica la resistencia al cambio de pH observada en la gráfica.
Región III: Punto medio de la titulación (12.5 mL)
Este punto se localiza en el centro de la zona amortiguadora. Cuando las concentraciones de ácido y base conjugada son iguales, el pH depende exclusivamente de la constante del ácido. Este punto es fundamental porque define la capacidad amortiguadora máxima del sistema y sirve como referencia experimental para determinar pKa.
Región IV: Punto de equivalencia (25.0 mL)
Se observa un cambio pronunciado en la pendiente, es el punto de equivalencia. Todo el ácido ha reaccionado, pero el pH no es neutro. La tabla muestra que la única especie relevante es la base conjugada (A⁻), la cual sufre hidrólisis básica, elevando el pH por encima de 7.
Región V: Después del punto de equivalencia
La curva se vuelve nuevamente menos inclinada, pero en valores altos de pH. Una vez consumido todo el ácido, el pH está controlado exclusivamente por el exceso de base fuerte añadida y la presencia del ácido deja de ser relevante frente a la alta concentración de OH⁻, lo cual se refleja en el aumento rápido del pH.
Caso 2: Ácido diprótico (H₂A) — estructura + interpretación
Al titular un ácido diprótico débil (H₂A) con una base fuerte, observamos dos transiciones químicas secuenciales, correspondientes a la neutralización de cada protón. Esto se traduce en dos zonas amortiguadoras y dos puntos de equivalencia en la curva.
Ejemplo General
Analito: 25.0 mL de ácido diprótico débil H₂A (0.10 M).
Titulante: Base fuerte OH⁻ (0.10 M).
Constantes: pKa₁ ≈ 2.0, pKa₂ ≈ 5.0.
Volúmenes clave (por estequiometría):
- 1er P.E. (neutralización a HA⁻): 25.0 mL
- 2do P.E. (neutralización a A²⁻): 50.0 mL
En este caso hay que adaptar la Tabla de Variación de Composición
Esta se extiende añadiendo filas para capturar la segunda etapa de la reacción. La tabla tendrá a las especies H₂A, HA⁻, A²⁻, OH⁻, y también recorre más etapas: desde el inicio con solo H₂A, pasando por la primera zona amortiguadora (donde coexisten H₂A y HA⁻), el primer punto de equivalencia (donde predomina HA⁻), la segunda zona amortiguadora (con HA⁻ y A²⁻), el segundo punto de equivalencia (con A²⁻), y finalmente la región de exceso de base.
Características de la curva para ácido diprótico
Al unir estos puntos con una línea suave, obtenemos una curva con dos "escalones" distinguibles, siempre que los pKa estén suficientemente separados:
1. Primera Meseta (pH ~2-4): Corresponde a la zona del primer amortiguador (H₂A/HA⁻), centrada en pH ≈ pKa₁.
2. Segunda Meseta (pH ~4.5-6): Corresponde a la zona del segundo amortiguador (HA⁻/A²⁻), centrada en pH ≈ pKa₂.
3. Dos Saltos de pH:
- El primero, menos pronunciado, en el 1er P.E. (~25 mL)
- El segundo, más brusco y alcalino, en el 2do P.E. (~50 mL), confirmando la neutralización completa a A²⁻
Regiones de la titulación de ácido diprótico
Región I: Inicio de la titulación (0 mL)
Solo está presente la especie H₂A. El pH inicial es ácido moderado debido a la disociación parcial del primer protón. La pendiente es suave, ya que el equilibrio ácido–base limita la concentración de H⁺.
Región II: Primera zona amortiguadora (antes del primer PE)
La solución contiene cantidades comparables de H₂A y HA⁻. La curva presenta una pendiente pequeña debido al efecto amortiguador. En el punto medio de esta región, donde [H₂A] = [HA⁻], se cumple que pH = pKa₁.
Región III: Primer punto de equivalencia (25.0 mL)
Todo el H₂A ha sido convertido en HA⁻. La especie HA⁻ es anfiprótica, por lo que el pH resulta intermedio y depende tanto de Ka₁ como de Ka₂. La pendiente aumenta, marcando el final de la primera neutralización.
Región IV: Segunda zona amortiguadora
En esta región coexisten HA⁻ y A²⁻. El sistema vuelve a mostrar capacidad amortiguadora. En el punto medio de esta región se cumple que [HA⁻] = [A²⁻], por lo que el pH es igual a pKa₂.
Región V: Segundo punto de equivalencia (50.0 mL)
Todo el ácido ha sido completamente desprotonado y la especie predominante es A²⁻. Esta especie sufre hidrólisis básica, lo que provoca un pH mayor que 7. La pendiente vuelve a incrementarse de forma notable.
Región VI: Después del segundo punto de equivalencia
El pH está gobernado exclusivamente por el exceso de base fuerte añadida. La química del ácido deja de influir y la curva se comporta de manera similar a una disolución de base fuerte diluida.
Por último la forma característica de una curva de titulación no es arbitraria, sino que surge directamente de los equilibrios químicos que dominan en cada etapa del proceso. Al analizar la titulación mediante la tabla de variación de composición, se identifica que cada región de la curva corresponde a un conjunto distinto de especies predominantes en disolución.
- En el inicio, la pendiente es suave debido a la disociación parcial del ácido, lo que limita el cambio de pH.
- Antes del punto de equivalencia, la coexistencia del ácido y su base conjugada genera una región amortiguadora, responsable de la resistencia al cambio de pH y del tramo casi horizontal de la curva.
- El punto de equivalencia se manifiesta como un cambio brusco en la pendiente porque ocurre la neutralización estequiométrica completa del analito, dando lugar a una especie cuya hidrólisis modifica significativamente el pH.
- Finalmente, después del punto de equivalencia, el exceso de titulante controla el pH de la disolución y la curva vuelve a presentar una pendiente más moderada.
Método 2: Interpretación por Especies
Este método de diagramas de distribución de especies también conocido como gráficas α, es una herramienta gráfica que permite interpretar una curva de titulación desde el punto de vista que nos permite ver qué especies químicas predominan en la disolución a cada valor de pH.
Este método se fundamenta exclusivamente en el equilibrio ácido–base y en el valor de la constante de acidez del analito. Este enfoque no se utiliza principalmente para calcular el pH de una disolución, sino para:
- Comprender la estructura de la curva de titulación
- Identificar regiones de amortiguamiento
- Localizar puntos característicos como el pKa
- Explicar por qué la curva presenta ciertos cambios de pendiente
Procedimiento general
1. Definir el sistema químico
Se considera un ácido débil general:
- HA para un ácido monoprótico
- H₂A para un ácido diprótico
Y se conocen sus constantes de acidez:
- Para monoprótico: Ka
- Para diprótico: Ka₁ y Ka₂
2. Expresar las fracciones de distribución (α)
Para cada especie presente en el sistema, se define una fracción α que representa la proporción de esa especie respecto al total del analito.
α_HA = [H⁺] / ([H⁺] + Ka)
α_A⁻ = Ka / ([H⁺] + Ka)
Donde: Ka = 10-pKa = 10-5.00
Estas fracciones dependen únicamente del pH y de las constantes de equilibrio.
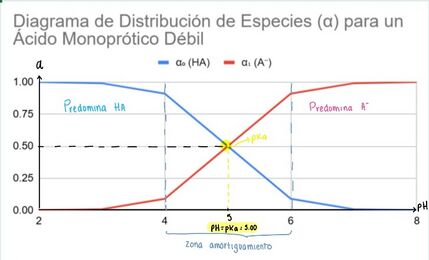
3. Construir el diagrama e interpretarlo
Se grafican las fracciones α en función del pH:
- Eje vertical: Fracción α (de 0 a 1)
- Eje horizontal: pH
El predominio de una especie sobre las demás define regiones, que pueden relacionarse directamente con las distintas zonas de la curva de titulación.
Estos diagramas permiten explicar:
- Por qué la curva de titulación presenta una pendiente suave antes del punto de equivalencia
- Por qué el pKa puede identificarse gráficamente en el punto medio de la titulación
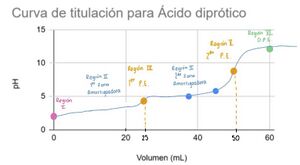
Representación visual de la curva de tutulación para un Ácido monoprótico. Se muestra la variación del pH en función del volumen de base fuerte añadida durante la titulación de un ácido monoprótico débil genérico (HA).
2: Construir la tabla de datos
| pH (Columna 1) |
[H⁺] = 10-pH (Columna 2) |
αHA (Columna 3) |
αA⁻ (Columna 4) |
Interpretación (Columna 5) |
|---|---|---|---|---|
| 2 | 1.00 × 10-2 | 0.999 | 0.001 | A pH muy bajo, HA domina absolutamente (~99.9%) |
| 3 | 1.00 × 10-3 | 0.990 | 0.010 | HA aún domina fuertemente |
| 4 | 1.00 × 10-4 | 0.909 | 0.091 | HA predomina, pero A⁻ ya aparece (~9%) |
| 5 | 1.00 × 10-5 | 0.500 | 0.500 | ¡Punto de cruce! αHA = αA⁻ = 0.5 pH = pKa |
| 6 | 1.00 × 10-6 | 0.091 | 0.909 | A⁻ ahora predomina claramente (~91%) |
| 7 | 1.00 × 10-7 | 0.0099 | 0.9901 | A⁻ domina fuertemente |
| 8 | 1.00 × 10-8 | 0.001 | 0.999 | A pH alto, A⁻ domina absolutamente (~99.9%) |
Guía para llenar cada columna
Columna 1 - Valores de pH elegidos: Son los puntos del eje horizontal que queremos representar. Elegimos un rango que cubra desde donde el ácido está completamente protonado (pH bajo) hasta donde está completamente desprotonado (pH alto), centrándonos alrededor del pKa.
Columna 2 - Concentración de H⁺ ([H⁺]): Viene de la definición fundamental del pH: [H⁺] = 10-pH
Columnas 3 y 4 - Fracciones Molares (αHA y αA⁻): Surgen de los coeficientes de distribución del sistema, que se derivan del equilibrio HA ⇌ H⁺ + A⁻ y el balance de masa. Para el cálculo basta con sustituir el [H⁺] de la columna 2 y el valor de Ka (10-pKa) en estas fórmulas.
Columna 5 - Interpretación (Predicción):
Si [H⁺] ≫ Ka (pH bajo): El denominador ([H⁺] + Ka) estará dominado por [H⁺].
Si [H⁺] ≈ Ka (pH cercano al pKa): Ambas especies contribuyen.
Cuando [H⁺] = Ka exactamente (pH = pKa), αHA = αA⁻ = 0.5.
Si [H⁺] ≪ Ka (pH alto): El denominador estará dominado por Ka.
Paso 3: Dibujar el Diagrama a Mano
1. Dibuja los ejes:
- Eje X (Horizontal): "pH" – Aquí estarán los valores de pH (de 2 a 8)
- Eje Y (Vertical): "Fracción Molar (α)" – Marcado de 0 a 1
2. Graficar puntos:
- Para αHA: Grafica los puntos:(pH=2, α=0.999),(pH=4, α=0.909),(pH=5, α=0.5),(pH=6, α=0.091) y(pH=8, α=0.001)
- Para αA⁻: Grafica los puntos:(pH=2, α=0.001),(pH=4, α=0.091),(pH=5, α=0.5),(pH=6, α=0.909)y (pH=8, α=0.999)
3. Unir los puntos con curvas suaves:
- La curva de αHA comenzará casi en 1 a la izquierda (pH bajo) y descenderá suavemente en forma de "S" tendida hasta casi 0 a la derecha (pH alto).
- La curva de αA⁻ es complementaria: comenzará casi en 0 a la izquierda y ascenderá suavemente en forma de "S" hasta casi 1 a la derecha.
- Ambas curvas se cruzan exactamente en el punto (pH=5, α=0.5).
Paso 4: Interpretación del Diagrama en el Contexto de una Titulación
¿Dónde y cómo se "ve" el PE en el diagrama? El punto de equivalencia (PE) ocurre cuando se ha añadido la cantidad estequiométricamente exacta de base para convertir todo el HA inicial en A⁻. En el diagrama, esto se traduce en:
- Para αA⁻ (la especie producto): El PE ocurre en el punto donde la curva de αA⁻ alcanza (o se acerca asintóticamente a) su valor máximo de 1. En ese instante, la fracción de A⁻ es prácticamente del 100%.
- Para αHA (la especie analito): Simultáneamente, es el punto donde la curva de αHA llega (o se acerca asintóticamente a) 0. La fracción de HA es prácticamente nula.
Interpretación por etapas
Al inicio de la titulación (pH bajo = 2-3): En el extremo izquierdo, la curva de HA está pegada a 1. Esto significa que la disolución es prácticamente 100% HA y casi nada de A⁻, lo que corresponde al inicio de la titulación.
Al añadir base y acercarse al punto de semi-equivalencia (pH ~5): En el centro del gráfico, las dos curvas se cruzan en α = 0.5. Esto significa que HA y A⁻ están presentes en concentraciones exactamente iguales. Esta es la definición del punto de semi-equivalencia. Aquí, la disolución es un amortiguador (por eso en la curva de titulación hay una zona plana). El diagrama muestra que este momento ocurre exactamente a pH = pKa.
Al pasar el punto de equivalencia (pH alto = 8): En el extremo derecho del gráfico, la curva de A⁻ está pegada a 1. Esto significa que prácticamente todo el HA se ha convertido en A⁻. La disolución ahora se comporta como una solución de la base débil A⁻ (que se hidroliza, dando un pH > 7).
Extensión a sistemas más complejos Este método nos permite usar el diagrama de distribución como un mapa químico que conecta directamente los equilibrios ácido–base con la forma de la curva de titulación.
Para sistemas más complejos, como ácidos dipróticos
IMAGENNN DIAGRAMA 2
- Se notandos puntos de cruce muy claros a α = 0.5: uno en pH correspondiente a pKa₁ y otro en pH correspondiente a pKa₂.
- La curva de HA⁻ forma una campana prominente entre los dos puntos de cruce. Esto visualiza la zona donde el anfolito es la especie principal.
- La aparición de especies adicionales y de múltiples cruces refleja la existencia de varias regiones amortiguadoras y de más de un punto de equivalencia en la titulación.
Método 3: Diagrama Logarítmico
Este método se basa en la representación gráfica del logaritmo de la concentración de cada especie química en función del pH, lo que permite identificar de manera directa las especies predominantes y las regiones químicas que explican la forma de la curva de titulación.
Procedimiento del método
Paso 1. Identificación del sistema químico En primer lugar, se identifica el tipo de analito que se desea estudiar:
- Para un ácido monoprótico: se considera la especie general HA
- Para un ácido diprótico: se emplea la forma H₂A
Posteriormente, se identifican las constantes de acidez correspondientes:
- Caso monoprótico: un único pKa
- Caso diprótico: pKa₁ y pKa₂
Estas constantes determinan los valores de pH en los que cambia la especie predominante.
Paso 2. Construcción del diagrama log C vs pH En el diagrama logarítmico:
- Eje horizontal: pH
- Eje vertical: logaritmo de la concentración (log C) de cada especie química
Cada especie se representa mediante una recta cuya pendiente y posición dependen del equilibrio ácido–base. Los puntos de intersección entre rectas indican condiciones en las que dos especies tienen concentraciones iguales.
Para ácido monoprótico:
- La intersección entre log[HA] y log[A⁻] ocurre en pH = pKa
Para ácido diprótico: Aparecen dos intersecciones: 1. En pH = pKa₁: donde [H₂A] = [HA⁻] 2. En pH = pKa₂: donde [HA⁻] = [A²⁻]
Estas intersecciones delimitan regiones químicas bien definidas.
Paso 3. Introducción de la línea de concentración analítica total
Una característica esencial del método es la introducción de una línea horizontal que representa el logaritmo de la concentración analítica total del ácido:
Error al representar (MathML con SVG o PNG como alternativa (recomendado para navegadores modernos y herramientas de accesibilidad): respuesta no válida («Math extension cannot connect to Restbase.») del servidor «https://wikimedia.org/api/rest_v1/»:): {\displaystyle \log C_T} donde Error al representar (MathML con SVG o PNG como alternativa (recomendado para navegadores modernos y herramientas de accesibilidad): respuesta no válida («Math extension cannot connect to Restbase.») del servidor «https://wikimedia.org/api/rest_v1/»:): {\displaystyle C_T = [\text{HA}] + [\text{A}^-]}
Esta línea no proviene del equilibrio químico, sino de los datos del problema de titulación. Su función es conectar el diagrama teórico con la situación real del sistema. La comparación entre esta línea y las rectas de las especies permite identificar directamente cuál especie predomina en cada intervalo de pH.
| Diagrama logarítmico | Curva de titulación | Especies predominantes | Región de la titulación |
|---|---|---|---|
| log[HA] cerca de log CT log[A⁻] muy por debajo |
Pendiente suave | HA o H₂A | Inicio de la titulación |
| log[HA] ≈ log[A⁻] ≈ log CT | Zona casi horizontal | Dos especies comparables | Zona amortiguadora |
| Intersección de rectas (cambio de predominio) |
Cambio brusco de pendiente | Cambio brusco de predominio | Punto de equivalencia |
| log[A⁻] cerca de log CT log[HA] muy por debajo |
Pendiente moderada | A⁻ o A²⁻ | Después del PE |
Ejemplo: Ácido monoprótico
Diagrama hipotético
Consideremos un ácido monoprótico con:
- n = 1 (monoprótico)
- pKa = 5
- Co = 0.1 mol/L
DIAGRAMa
Nota: En esta presentación se omiten las líneas correspondientes a H⁺ y OH⁻ para enfatizar el uso del diagrama como herramienta de identificación de especies predominantes y regiones de titulación, que es el objetivo principal del método.
Interpretación por regiones y relación con la curva de titulación
1. pH < pKa (pH < 5):
- La recta correspondiente a log[HA] se encuentra por encima de la de log[A⁻]
- log[HA] es la más cercana a la línea log CT
- Especie predominante: ácido no disociado HA
- Asociación con curva: Inicio de la titulación
- Comportamiento: Sistema controlado por el ácido débil sin neutralizar
- Reflejo en curva: Pendiente relativamente suave
2. pH ≈ pKa (pH ≈ 5):
- Ambas curvas se intersectan exactamente en pH = pKa = 5
- La línea log CT pasa cerca de este punto de intersección
- Las concentraciones de HA y A⁻ son comparables
- Propiedad: Máxima capacidad amortiguadora del sistema
- Asociación con curva: Punto medio de la titulación
- Característica: Pequeños cambios en titulante → variaciones mínimas de pH
- Relación: pH ≈ pKa
3. pH > pKa (pH > 5):
- La recta de log[A⁻] domina el diagrama
- log[A⁻] es la más cercana a la línea de concentración total log CT
- Especie predominante: base conjugada A⁻
- Asociación con curva: Zonas cercanas o posteriores al punto de equivalencia
- Estado del sistema: Ácido ha reaccionado casi por completo
- Control del pH: Especies básicas (A⁻ y posible exceso de titulante)