Relaciones cuantitativas en sistemas redox: Enfoque – Potencial de electrones
Revisión del 17:41 15 ene 2026 de AlejandroGuerrero (discusión | contribs.) (Página creada con «Aquí es necesario plantear un equilibrio considerando una ''concentración de electrones''. Para una reacción de la forma:<chem display="block">a A + n e^- <=> b B + c C</chem>Planteamos la constante de equilibrio y luego despejamos a la concentración de electrones <math>[e^{-}]</math>para aplicarle el cologaritmo correspondiente. Así obtenemos un ''potencial de electrón'' <math>pe^{-}</math>de tal manera que...<math display="block">pe^{-} =\log_{10}{\frac{K_{eq}…»)
Aquí es necesario plantear un equilibrio considerando una concentración de electrones. Para una reacción de la forma:
Planteamos la constante de equilibrio y luego despejamos a la concentración de electrones para aplicarle el cologaritmo correspondiente. Así obtenemos un potencial de electrón de tal manera que...
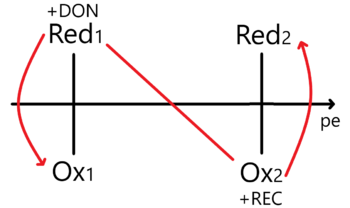
Al hacer esto le estamos dando un tratamiento termodinámico. Ahora tenemos que representarlo en el DUZP.
La relación entre el potencial de electrones y el estándar de reducción viene dada por la ecuación:
Siguiente página: Relaciones cuantitativas en sistemas redox: Enfoque – Potencial estándar de reducción

![{\displaystyle [e^{-}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/417d75f02ae885550bb2a7b50ac4cc5b3a770c10)

![{\displaystyle pe^{-}=\log _{10}{\frac {K_{eq}}{n}}+\log _{10}{\frac {[A]^{a}}{[B]^{b}[C]^{c}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cc0b592017e699c50d97c18c32418b50ef1e27d7)