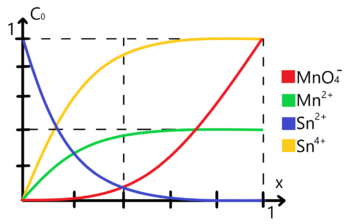
Gráfico de variación de concentraciones respecto al avance de reacción para la titulación de una solución de estaño con permanganato
Para ejemplificarlo supongamos un sistema donde usamos permanganato para valorar o titular una solución de iones de estaño para lo cual consideramos los potenciales estándar de reducción para cada una de las especies involucradas; la propia facultad de química de la UNAM tiene una tabla con los valores de potenciales estándar de reducción para muchas especies distintas para lo cual consideraremos los valores de +1.51 eV para el par y de +0.15 eV para el par .
Entonces las semirreacciones a considerar son:
Entonces planteamos la siguiente reacción:
Si tienes dudas sobre cómo llegamos a esta conclusión considera revisar el tema balanceo ion electrón.
Para encontrar un gráfico de la variación de las especies implicadas respecto al avance de la reacción es necesario antes realizar la tabla y analizarla. A continuación te muestro dicha tabla simplificada (eliminamos a la concentración de protones porque decido ignorar el pH, así como la de agua porque asumimos que se encuentra en exceso):
Si deseas profundizar sobre cómo realizar este tipo de tablas considera revisar el tema tabla de variación de especies. Con la ayuda de esta tabla podemos realizar un gráfico que nos muestre cómo varía la concentración de cada una de las especies involucradas respecto al avance de la reacción tal, para ello tienes que considerar los siguientes puntos representándolos en el gráfico:
- Al inicio del sistema () sólo existe el analito Sn(2+) en el mismo en una concentración analítica dada (). Si bien esta se encuentra en equilibrio con una cantidad dada de Sn(4+) esta está presente en cantidades despreciables por ahora. Entonces colocaremos un punto azul en la coordenada (0,1).
- Aún en el inicio del sistema contemplamos que no hay ni una pizca de permanganato y mucho menos de ion manganeso, entonces colocamos puntos rojos y verdes en la coordenada (0,0).
- Conforme añadimos valorante (permanganato) el Sn(2+) se consume progresivamente y el permanganato totalmente (reacciona "casi" por completo) hasta alcanzar una paridad equimolar entre el titulante y el analito. Mientras este proceso ocurre decimos que estamos "Antes del Punto de Equivalencia" o A.P.E. y, cuando finalmente lo hemos alcanzado, estamos en el "Punto de Equivalencia" o P.E.
- En el P.E. () asumiremos que las cantidades de analito y titulante son despreciables por ahora () aunque no necesariamente igual de insignificante a como lo estaba en Sn(4+) al principio del proceso, por eso manejamos distintas épsilon. Entonces colocaremos los puntos correspondientes en (,0) para estas dos especies.
- Por otro lado, los productos de esta titulación deberían de haber alcanzado concentraciones equimolares respecto a lo añadido hasta ahora de titulante, de acuerdo a la tabla de variación de especies realizada anteriormente podemos ver que en este punto debería de haber de Mn(2+) así como de de Sn(4+). Colocaremos los puntos correspondientes a una distancia de .
- "Después del Punto de Equivalencia" o D.P.E. no podremos generar más productos simplemente añadiendo más titulante, por lo que la concentración de estos permanece prácticamente constante así como lo que restaba de analito.
- Lo que sí varía es la concentración de titulante añadido, diremos que habremos de añadir suficiente hasta lograr igualar su concentración respecto a la que había originalmente de analito (). Entonces le colocamos su respectivo punto en la coordenada (1,1).
- Finalmente unimos los puntos mediante líneas rectas, esta gráfica quedaría lista si tan sólo las cantidades fueran realmente insignificantes, algo curioso de la Química Analítica es que lo son hasta que de pronto dejan de serlo y este es uno de esos casos jaja. El gráfico que generaste con líneas rectas sólo aplica en reacciones completas y no en equilibrios químicos, entonces para corregirlo basta con "suavizar" tales líneas a curvas y comprender que esto sucede porque el sistema "siempre tiende a un equilibrio químico" de concentraciones; nota que en el P.E. si bien deberían de haberse consumido los reactivos, gracias a nuestro gráfico suavizado podemos apreciar que realmente aún están presentes aunque en cantidades "pequeñas".
Ahora que tenemos este gráfico es necesario generar uno que muestre la variación del potencial de reducción respecto al avance de reacción. Ya tenemos la mitad del trabajo hecho pues conocemos la tabla de variación de especies y con esta misma podemos obtener el potencial de reducción del sistema en cualquier momento dado simplemente aplicando la ecuación de Nernst.
Nótese que aparecen amortiguadores cuando y .


















![{\displaystyle {\ce {[Sn^{2+}] = [Sn^{4+}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e5c473e92e5fe7ae452402cc5d0c5c68046230fc)
![{\displaystyle {\ce {[ MnO4^{1-}] = [ Mn^{2+}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6bb3a45e58c8499d9e30b8167f5c0fcb1955adbf)