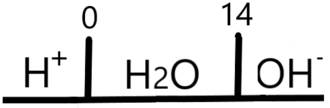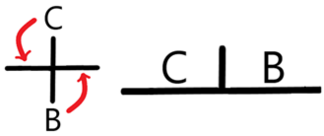Diagramas Unidimensionales de Zona de Predominio (DUZP)
Introducción
Estos diagramas resultan útiles para predecir reacciones y plantear zonas de predominio en sistemas donador-receptor donde existe un Donador (puede ser un agente Reductor, un ácido o un complejo de coordinación) de partícula P (puede ser un electrón e-, un protón H+ o un ligante L) la cual la recibe un Receptor (puede ser un agente Oxidante, una base o un catión metálico M).
Estos diagramas se trazan mediante una escala de potencial de partícula a lo largo de lo cual trazamos a los donadores y a los receptores según su fuerza de intercambio de partícula, para esto es necesario conocer los siguientes datos:
- La o las reacciones de intercambio de partícula
- La fuerza relativa del intercambio, la cual puede ser
- El potencial de electrón pe- o el potencial estándar de reducción Eo
- La constante de disociación ácida Kaj o de formación global βj
- La constante de formación Kfn o de formación global βn
Tal información suele estar reportada en la bibliografía, a continuación se enlistan algunas tablas disponibles en el AMyD de la Facultad de Química, UNAM:
- Manual de química analítica [1]
- Tabla de datos de pKa y Eo bioquímicos[2][3]
- Formación de complejos en química analítica[4]
- pKa compilada por R. Williams[5]
Diagramas de predicción de reacción
Para construir un DUZP antes es necesario plantear un diagramas de predicción de reacción para lo cual es necesario seguir los siguientes pasos:
- Trazar una línea recta horizontal (aunque bien se puede hacer vertical) la cual servirá como nuestro eje "p" de partícula pP (done "p" viene del cologaritmo -log aplicado a la concentración de partícula P). Esta servirá para ubicar a los pares donador-receptor según su fuerza relativa.
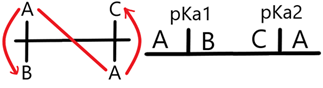
- Identificar los pares donador-receptor dada su fuerza relativa, esta variará de tal forma que a menor pP mayor será su fuerza de intercambio y viceversa, a mayor pP menor será su fuerza. Para ejemplificar hemos de plantear dos equilibrios con sus respectivas fuerzas.Supongamos que pP1 < pP2 esto es Donador1 es más fuerte que Donador2.
- Ubicar a los pares en la escala pP según su fuerza relativa de izquierda a derecha colocando a las especies donadoras en la parte superior y a las receptoras en la inferior.Esto puede hacerse para uno o más, tantos pares como todos los que participen en tu sistema en cuestión siempre y cuando todos intercambien el mismo tipo de partícula (no puedes mezclar equilibrios simultáneos para el mismo DUZP).
- Identificar a los donadores más fuertes así como a los receptores. Para esto hemos de leer la escala superior de izquierda a derecha en orden decreciente de fuerza y viceversa a la escala inferior para los cuales el orden es creciente, entonces llegamos a la conclusión de que el Donador1 es el más fuerte, mientras que el Receptor2 es el más fuerte.
- Identificar a los pares reaccionantes dada la máxima "el donador más fuerte reacciona con el receptor más fuerte", estas reacciones reaccionan espontáneamente en la disolución para dar a sus respectivas contrapartes respetando algo conocido como la regla de la N debido a la forma que dan las flechas que dirigen a las especies reaccionantes. En este caso Donador1 reacciona con Receptor2 para formar Receptor1 y Donador2.
- Calcular la constante de reacción para el nuevo equilibrio considerando la distancia entre ambos pares implicados, esta distancia corresponde a la diferencia de p de partícula ΔpP correspondiente a la reacción de interés.Resulta fácil eliminar el cologaritmo si se requiere abordar algebraicamente el equilibrio. A estas alturas contamos con la reacción de interés y su constante de equilibrio.
Diagrama Unidimensional de Zona de Predominio (DUZP)
Trazar un DUZP resulta sencillo comprendiendo cómo trazar un diagrama de predicción de reacciones teniendo en cuenta que estos se harán para sistemas más simples. Por ejemplo, considere las siguientes reacciones sucesivas donde Don se refiere a la especie donadora de P partículas:
Aplicaremos la regla de la N enfocándonos en el eje pP, nótese que hay zonas donde las mismas especies coinciden y esto se debe a que se tratan de anfolitos estables.
Entonces el DUZP queda como:
Cabe recalcar que los DUZP sólo se hacen para una sola especie y sus reacciones sucesivas (deprotonaciones por ejemplo).
Sistemas Donador-Receptor de partícula
Estudiaremos tres sistemas distintos a lo largo de la asignatura.
Sistemas óxido-reducción
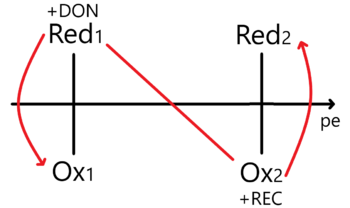
Enfoque en el potencial de electrones
Aquí es necesario plantear un equilibrio considerando una concentración de electrones. Para una reacción de la forma:
Planteamos la constante de equilibrio y luego despejamos a la concentración de electrones [ e- ] para aplicarle el cologaritmo correspondiente. Así obtenemos un potencial de electrón pe- de tal manera que...
Al hacer esto le estamos dando un tratamiento termodinámico. Ahora tenemos que representarlo en el DUZP.
Si bien este modelo está alineado al enfoque en los equilibrios según la interacción donador-receptor, normalmente en la bibliografía no se abordan los equilibrios óxido-reducción de esta manera sino enfocándose en el potencial estándar de reducción. La relación entre el potencial de electrones y el estándar de reducción viene dada por la ecuación:
Enfoque en el potencial estándar de reducción
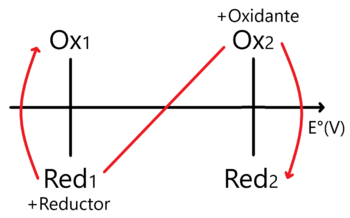
En este caso la regla de la N se invierte dado que ahora ubicamos a los donadores en la escala inferior y a los receptores en la superior, este enfoque es bastante usado en la enseñanza.
Nótese que en este caso ubicamos al Oxidante más fuerte en la parte superior derecha y al Reductor más fuerte en la inferior izquierda. En este sentido encontraremos el Proceso Espontáneo y cuya constante de equilibrio se encuentra como:
Donde hemos de sustituir n por el número de electrones intercambiados según la reacción de óxido-reducción completa, esto también es el mínimo común múltiplos de los electrones intercambiados, n1 y n2, por semirreación:
Sistemas ácido-base
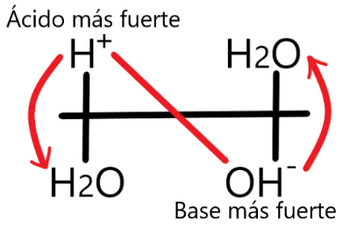
El DUZP se construye ordenando a los pares ácido-base según sus valores de pKa ubicando a los donadores de protones o ácidos (H+) por encima y a los receptores o bases por debajo de la recta. En los extremos de la recta colocamos a los pares ácido-base del agua coronándolos como los más fuertes en su categoría y marcándolos como límites de la misma (0 y 14, de acuerdo al pH).
Siguiendo la regla de la N se obtiene el proceso más termodinámicamente favorable y cuya constante de reacción (Kr) se define como:
Si la reacción a estudiar sigue una dirección opuesta a esta regla entonces estará ante un proceso termodinámicamente desfavorecido cuya Kr se invierte.
Anfolitos inestables
Puede suceder (y lo hará) que aparezcan anfolitos inestables, en ese caso deberá de eliminarlos antes de proceder de cualquier forma. Sabes que hay uno cuando el DUZP muestra a la misma especie en dos zonas distintas o bien que la reacción entre sus especies es termodinámicamente favorable.
Así se ve el DUZP del agua:
Nótese que no tiene anfolitos inestables. Ahora así se ve uno que sí los tiene:
Nótese la aberración en el diagrama. Para resolverlo tenemos que plantear la reacción del anfolito y obtenemos la media de sus pKa con un análisis de reactividad. Entonces…
Conversión de pOH a pH en un DUZP
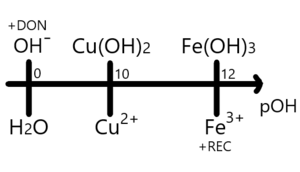
A veces resulta necesario trabajar el DUZP en una escala de pOH en lugar de pH lo cual implica intercambiar partículas hidróxido (OH-), para esto es importante recordar la relación:
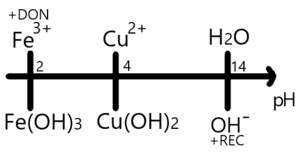
El donador más fuerte de partícula sigue encontrándose en el extremo superior izquierdo mientras que el receptor más fuerte lo está en el inferior derecho. Al hacer el cambio de escala también cambia el orden de las especies invirtiéndose completamente, tanto de izquierda a derecha como de arriba hacia abajo, por ejemplo así se vería el cambio de escala para una serie de hidróxidos de hierro y cobre en medio acuoso:
Sistemas complejos
(No es la prio, enfocarse en lo que ya está)
- ↑ Lurie. (1975). Handbook of Analythical Chemistry (N. Bobrov, Trad.; 1.a ed.). Mir Publishers.
- ↑ Cooper, T. (1977). Ion specific electrodes: The tools of biochemistry. John Wiley & Sons.
- ↑ H. Segel, I. (1981). Cálculos de bioquímica. Editorial Acribia. Zaragoza. España.
- ↑ Ringbom, A. (s. f.). Formación de complejos en química analítica. Alhambra.
- ↑ Williams, R. (s. f.). pKa data compiled by R. Williams.
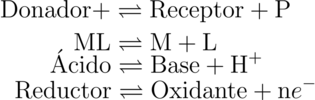















![{\displaystyle p{\text{e}}^{-}=\log _{10}{\frac {K_{eq}}{n}}+\log _{10}{\frac {[{\text{A}}]^{a}}{[{\text{B}}]^{b}[{\text{C}}]^{c}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89b0409e4fe64a313c49a7c272e699592e36e7f1)