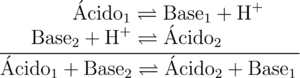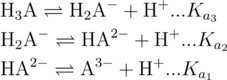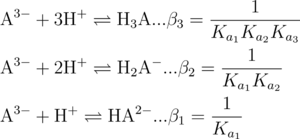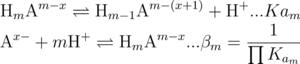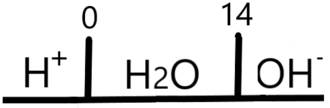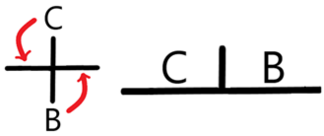Equilibrios Ácido-Base
Introducción a los equilibrios ácido-base
(Añadir en Redox forma trad de hacer un DUZP y la nueva en función de DON y REC)
Estudiaremos a los equilibrios ácido-base como un sistema de intercambio de partícula de manera muy similar a como estudiamos a los equilibrios óxido-reducción, sólo que esta vez intercambiamos protones (H+) en lugar de electrones (e-). Entonces, apoyándonos en la teoría de los ácidos de Brönsted-Lowry, consideramos que un ácido es aquella especie capaz de ceder protones mientras que la base es aquella capaz de captarlos. Así el equilibrio de disociación ácida es:
Así, podemos definir al ácido muriático o clorhídrico (HCl) efectivamente como uno dado que en solución acuosa es capaz de ceder protones disociándose en iones cloruro (Cl-).
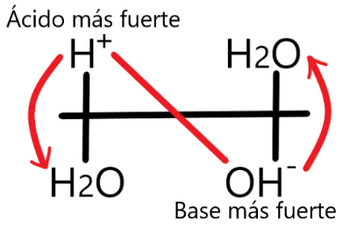
Al igual que los electrones resulta que los protones no pueden existir libres en una solución pues, mientras un ácido los cede es necesario una base que los fije. Entonces la reacción típica ácido-base es:
Si consideramos que este equilibrio está desplazado hacia la derecha entonces significa que el Ácido1 es más fuerte que el Ácido2 mientras que la Base2 es más fuerte que la Base1[1].
En disolución acuosa, el agua actúa como un ácido o una base débiles y de carácter opuesto a la especie que diluye (es un anfolito).
A la Base1 se le conoce como la base conjugada del Ácido1. De igual forma existe un ácido conjugado secundario a su respectiva base.
La acción del agua sobre el ácido se llama hidrólisis[1].
Si aplicamos la ley de acción de masas para encontrar la constante de equilibrio de esta reacción encontraremos que es[1]:
Nótese que estamos despreciando la concentración de agua en la solución (que en esencia es constante) pues la Kr ya la incluye.
Autodisociación del agua
El agua es un anfolito porque puede fijar como ceder protones según a que especie se encuentre, incluso puede reaccionar consigo misma manteniendo un equilibrio de autodisociación.
La constante de autodisociación del agua Kw realmente varía con la temperatura aunque su variación es mínima; tiene un valor de 10-13.98 a 25°C y de 10-14.2 a 18°C[1] aunque suele redondearse a 10-14.
Me quedé en la pg 32 de Charlot
Equilibrios de disociación sucesiva y de formación global
En relación con el empleo de las constantes de disociación, generalmente se utilizan las siguientes reacciones:
Donde Kam se refiere a la constante de acidez de la especie HmA que aún contiene m partículas de hidrógeno por liberar. Si m = 1 entonces estamos trabajando con un ácido monoprótico (ej. HCl, HF, HNO3, etc.), en cambio si m > 1 entonces estamos trabajando con ácidos polipróticos (H2SO4, H2SO4, H3PO4, H3Cit donde Cit se refiere al citrato).
Cuando trabajamos con ácidos polipróticos resulta conveniente trabajar con la constante de formación global para cada especie en lugar de las constantes de acidez debido a que ya las engloba. Estas constantes globales corresponden a las siguientes formaciones:
Donde βm se refiere a la constante global de formación para la especie HmA.
Estas constantes de acidez y de formación global podemos podemos generalizarlas de acuerdo a las ecuaciones:
Nota: No sé porqué no se actualiza la imagen!!!! Intenta cargar la imagen desde cero
Donde x se refiere a la carga de la base conjugada A como ion libre (totalmente desprotonado).
Diagrama Unidimensional de Zona de Predominio (DUZP)
(Esta podría ser una pg intermedia)
El DUZP se construye ordenando a los pares ácido-base según sus valores de pKa ubicando a los donadores de protones o ácidos (H+) por encima y a los receptores o bases por debajo de la recta. En los extremos de la recta colocamos a los pares ácido-base del agua coronándolos como los más fuertes en su categoría y marcándolos como límites de la misma (0 y 14, de acuerdo al pH).
Siguiendo la regla de la N se obtiene el proceso más termodinámicamente favorable y cuya constante de reacción (Kr) se define como:
Si la reacción a estudiar sigue una dirección opuesta a esta regla entonces estará ante un proceso termodinámicamente desfavorecido cuya Kr se invierte.
Anfolitos inestables
Puede suceder (y lo hará) que aparezcan anfolitos inestables, en ese caso deberá de eliminarlos antes de proceder de cualquier forma. Sabes que hay uno cuando el DUZP muestra a la misma especie en dos zonas distintas o bien que la reacción entre sus especies es termodinámicamente favorable.
Así se ve el DUZP del agua:
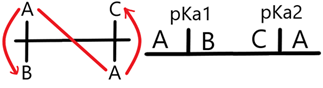
Nótese que no tiene anfolitos inestables. Ahora así se ve uno que sí los tiene:
Nótese la aberración en el diagrama. Para resolverlo tenemos que plantear la reacción del anfolito y obtenemos la media de sus pKa con un análisis de reactividad. Entonces…
Obteniendo así un nuevo diagrama sin el anfolito conflictivo.
Conversión de pOH a pH en un DUZP
A veces resulta necesario trabajar el DUZP en una escala de pOH en lugar de pH lo cual implica intercambiar partículas hidróxido (OH-), para esto es importante recordar la relación:
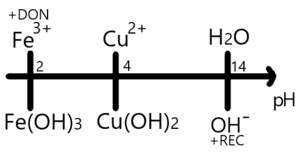
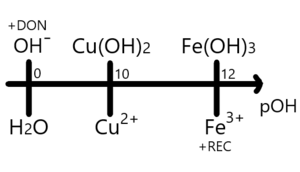
El donador más fuerte de partícula sigue encontrándose en el extremo superior izquierdo mientras que el receptor más fuerte lo está en el inferior derecho. Al hacer el cambio de escala también cambia el orden de las especies invirtiéndose completamente, tanto de izquierda a derecha como de arriba hacia abajo, por ejemplo así se vería el cambio de escala para una serie de hidróxidos de hierro y cobre en medio acuoso:
Ecuaciones de Charlotte
Aplican también para reacciones de intercambio de complejos y óxido-reducción simplemente comprendiendo que la especie donadora es el ácido y la receptora de partícula es la base.
Nota: Vale la pena añadir de dónde salen estas simplificaciones
Ácidos o donadores de partícula
- Ácidos fuertes o nivelados: Cumplen que α > 90% o bien Ka / Co ≥ 10, entonces:
Esta no es una simplif,
- Ácidos de fuerza media: Cumplen que 10% < α < 90% o bien 10-2 < Ka / Co < 10, entonces:
- Ácidos de fuerza débil: Cumplen que α < 10% o bien Ka / Co ≤ 10 -2, entonces:
Bases o receptores de partícula:
- Bases fuertes o niveladas: Cumplen que β > 90% o bien KaCo ≤ 10 -15, entonces:
- Bases de fuerza media: Cumplen que 10% < β < 90% o bien 10-15 < KaCo < 10-12, entonces:
- Bases de fuerza débil: Cumplen que β ≤ 10% o bien KaCo ≥ 10-12, entonces: