Equilibrios Ácido-Base
Introducción a los equilibrios ácido-base
Estudiaremos a los equilibrios ácido-base como un sistema de intercambio de partícula de manera muy similar a como estudiamos a los equilibrios óxido-reducción, sólo que esta vez intercambiamos protones (H+) en lugar de electrones (e-). Entonces, apoyándonos en la teoría de los ácidos de Brönsted-Lowry, consideramos que un ácido es aquella especie capaz de ceder protones mientras que la base es aquella capaz de captarlos. Así el equilibrio de disociación ácida es:
Ácido ⇌ Base + H+
Así, podemos definir al ácido muriático o clorhídrico (HCl) efectivamente como uno dado que en solución acuosa es capaz de ceder protones disociándose en iones cloruro (Cl-).
Al igual que los electrones resulta que los protones no pueden existir libres en una solución pues, mientras un ácido los cede es necesario una base que los fije. Entonces la reacción típica ácido-base es:
Ácido1 ⇌ Base1 + H+
Base2 + H+ ⇌ Ácido2
____________________
Ácido1 + Base2 ⇌ Ácido2 + Base1
Si consideramos que este equilibrio está desplazado hacia la derecha entonces significa que el Ácido1 es más fuerte que el Ácido2 mientras que la Base2 es más fuerte que la Base1[1].
En disolución acuosa, el agua actúa como un ácido o una base débiles y de carácter opuesto a la especie que diluye (es un anfolito).
Ácido1 + H2O ⇌ Base1 + H3O+
A la Base1 se le conoce como la base conjugada del Ácido1. De igual forma existe un ácido conjugado secundario a su respectiva base.
La acción del agua sobre el ácido se llama hidrólisis[1].
Si aplicamos la ley de acción de masas para encontrar la constante de equilibrio de esta reacción encontraremos que es[1]:
Nótese que estamos despreciando la concentración de agua en la solución (que en esencia es constante) pues la Kr ya la incluye.
Autodisociación del agua
El agua es un anfolito porque puede fijar como ceder protones según a que especie se encuentre, incluso puede reaccionar consigo misma manteniendo un equilibrio de autodisociación.
2 H2O ⇌ H3O+ + OH-
Kw = [H3O+][OH-] = 10-14
La constante de autodisociación del agua Kw realmente varía con la temperatura aunque es mínimo; tiene un valor de 10-13.98 a 25°C y de 10-14.2 a 18°C[1] aunque suele redondearse a 10-14.
El potencial de hidrógeno pH refiere al menos logaritmo de la concentraciones de iones hidronio en una solución, o sea queda definida por la siguiente relación[1]:
- pH = 7 para soluciones neutras
- pH < 7 para soluciones ácidas
- pH > 7 para soluciones básicas o alcalinas
Ecuación de Charlot
Suponga una solución con un ácido de la forma HA presente en una concentración c y la sal correspondiente MA (donde M es un metal) en una concentración c' y que se disocia totalmente. Existen pues el ácido HA y la base A- correspondientes. Después de un breve análisis podemos deducir la siguiente ecuación[1]:
Nótese que sólo se necesita conocer la constante de acidez Ka de la especie en cuestión así como de la concentración del ácido c y la base c' correspondiente para predecir el pH de la disolución.
Sea la fracción disociada o coeficiente de disociación α como el cociente entre el número de partículas disociadas respecto al número de partículas de partida sin disociar, podemos usar este parámetro para clasificar por su fuerza a las especies como fuertes o nivelados, de fuerza media o débiles de acuerdo a la tabla que se muestra a la derecha[1], donde Co es la concentración de la especie ácida y Ka su respectiva constante de acidez.
Derivado de esta ecuación es posible aproximarla a distintas situaciones concretas si se desea simplificar la ecuación, a continuación se muestran algunas de estas fórmulas así como otras tantas de interés. No está demás aclarar que estas ecuaciones y su deducción se encuentra en el capítulo 3 Ácidos y Bases de Química Analítica General Tomo I de Gaston Charlot.
Ácidos o donadores de partícula
- Ácidos fuertes o nivelados: Esta no es una aproximación, en su lugar es la definición de pH. Esto se cumple cuando el ácido HA se disocia prácticamente en su totalidad, o sea que cumplen que α > 90% o bien Ka / Co ≥ 10, entonces:
- Ácidos de fuerza media: Cumplen que 10% < α < 90% o bien 10-2 < Ka / Co < 10, entonces:
- Ácidos de fuerza débil: Cumplen que α < 10% o bien Ka / Co ≤ 10 -2, entonces:
Bases o receptores de partícula:
- Bases fuertes o niveladas: Cumplen que β > 90% o bien KaCo ≤ 10 -15, entonces:
- Bases de fuerza media: Cumplen que 10% < β < 90% o bien 10-15 < KaCo < 10-12, entonces:
- Bases de fuerza débil: Cumplen que β ≤ 10% o bien KaCo ≥ 10-12, entonces:
Anfolito Estable:
Cuando una especie se puede desempeñar tanto con carácter ácido como base y se encuentran en dismutación en equilibrio, entonces en el punto de equivalencia se cumple:
Amortiguadores - Ecuación de Henderson-Hasselbach:
Cuando tenemos una mezcla del ácido y la base conjugados, entonces formamos una disolución tampón o buffer y se caracteriza por la capacidad de no modificar notablemente el pH mientras se le añaden o eliminan iones H+. Para este tipo de amortiguadores se cumple la ecuación:
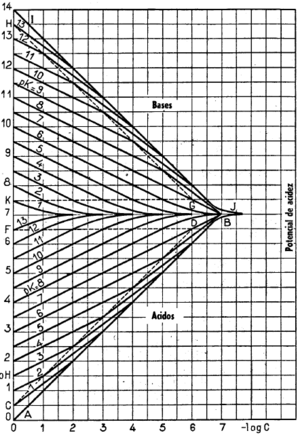
Gráfico de Flood
Permite encontrar el pH de las disoluciones en función de su concentración C y el pKa cualesquiera que sean las concentraciones[1], para usarlo es necesario comprender que el eje x corresponde al cologaritmo de la concentración del ácido o la base -log Co mientras que el eje y corresponde al potencial de acidez de acuerdo a los diferentes valores de pK.
Puedes hacer uso de la siguiente página para trabajar el diagrama de Flood.
Equilibrios de disociación sucesiva y de formación global
En relación con el empleo de las constantes de disociación, generalmente se utilizan las siguientes reacciones:
H3A ⇌ H2A- + H+ ... Ka3
H2A- ⇌ HA2- + H+ ... Ka2
HA2- ⇌ A3- + H+ ... Ka1
Donde Kam se refiere a la constante de acidez de la especie HmA que aún contiene m partículas de hidrógeno por liberar. Si m = 1 entonces estamos trabajando con un ácido monoprótico (ej. HCl, HF, HNO3, etc.), en cambio si m > 1 entonces estamos trabajando con ácidos polipróticos (H2SO4, H2SO4, H3PO4, H3Cit donde Cit se refiere al citrato).
Cuando trabajamos con ácidos polipróticos resulta conveniente trabajar con la constante de formación global para cada especie en lugar de las constantes de acidez debido a que ya las engloba. Estas constantes globales corresponden a las siguientes formaciones:
Donde βm se refiere a la constante global de formación para la especie HmA.
Estas constantes de acidez y de formación global podemos podemos generalizarlas de acuerdo a las ecuaciones:
Donde x se refiere a la carga de la base conjugada A como ion libre (totalmente desprotonado).
![{\displaystyle K_{r}={\frac {[{\text{Base}}][{\text{H}}_{3}{\text{O}}^{+}]}{[{\text{Ácido}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fd835cbcbf3670efa8c27409b3c1c420e3a63c11)
![{\displaystyle pH=-\log _{10}{[{\text{H}}_{3}{\text{O}}^{+}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/93c9bfa991c386697bd6f3ca0517bb3590325150)
![{\displaystyle [{\text{H}}^{+}]=K_{a}{\frac {c-[{\text{H}}^{+}]+[{\text{OH}}^{-}]}{c'+[{\text{H}}^{+}]-[{\text{OH}}^{-}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/742613694396dba6fc38ff65220d481df9bbe9b1)

![{\displaystyle pH=-\log _{10}{[{\text{H}}_{3}{\text{O}}^{+}]}=-\log _{10}{[{\text{H}}^{+}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2bf9d33d7cc871fba29e64cf10d86daaf4467c86)
![{\displaystyle [{\text{H}}^{+}]^{2}-K_{a}[{\text{H}}^{+}]-K_{a}C_{o}=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7e3a2ac24c0f0f513899f9867ad7bab073b0625e)

![{\displaystyle p{\text{H}}=14+\log _{10}{[{\text{OH}}^{-}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6a961bdf06711889905605f2f245d35652201503)
![{\displaystyle [{\text{H}}^{+}]^{2}C_{o}-K_{w}[{\text{H}}^{+}]-K_{a}K_{w}=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a2529c5b9b2ace6dcee00c9b442300d66b5c4d42)