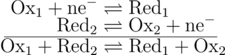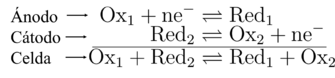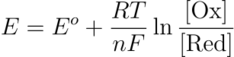Equilibrios de Óxido-Reducción
Introducción
Las reacciones de óxido-reducción son aquellas en las que ocurre un intercambio electrónico entre una oxidante capaz de fijar o "robar" electrones de un reductor que capaz de cedérselos[1], esta reacción química suele representarse de la siguiente manera:
Donde Ox se refiere a la especie Oxidante y Red a la Reductora.
Por ejemplo, podemos considerar al par Fe3+/Fe2+:
Donde el Fe3+ fija un electrón e- proveniente del Fe2+, entonces el Fe3+ se reduce (disminuye su estado de oxidación) y en consecuencia permite la oxidación de su contraparte por lo tanto es un agente Oxidante[1]. De la misma manera el Fe2+ se oxida (aumenta su estado de oxidación) permitiendo así la reducción de su contraparte por lo tanto es un agente Reductor[1].
Esto es una semirreacción de óxido-reducción y para completarla necesitamos de una semirreacción más pues los electrones no "viajan" libremente en la disolución (ni siquiera en el cableado eléctrico). Dadas dos semirreacciones estas se suman entre sí anulando la concentración de electrones brindándonos de una reacción completa de óxido-reducción:
Este tipo de procesos resultan más realistas y hasta reproducibles en laboratorio, por ejemplo en los electrodos de una celda electroquímica tenemos que el proceso de oxidación se lleva a cabo en el ánodo mientras que el reducción en el cátodo.
Ecuación de Nernst
Para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso Ox1 oxida a Red2 ya que Ox2 no puede oxidar a Red1; se dice entonces que Ox1 es un oxidante más fuerte que Ox2 al mismo tiempo que Red2 es un reductor más fuerte que Red1[2].
Para realizar tales predicciones de manera cuantitativa medimos el potencial estándar de reducción (E°) (REVISAAAAAR!!!!!!) para lo cual suponemos un sistema de dos semirreacciones (una de ellas estándar de valor 0 V y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la Ecuación de Nernst completa cuya forma es:
Donde
E°se refiere al potencial estándar de reducción[V] = VoltsRse refiere a la constante de los gases ideales[8.31446 J/mol*K]Tse refiere a la temperatura absoluta del sistema[K] = Kelvinnse refiere a la mol de electrones intercambiados por semirreacción[mol]Fse refiere a la constante de Faraday[e*NA=96485.33212 C/mol][Ox]y[Red]refieren a la concentración molar de cada especie oxidante y reductora[mol/L]
Si trabajamos en condiciones normales de temperatura (20 °C) y transformando el logaritmo natural a uno base diez podemos aproximar a la ecuación de Nernst simplificada:
El valor constante de 0.058 suele redondearse a 0.06 según cuanta precisión se desee. En caso de que el sistema esté representado por
Entonces la ecuación se adapta como:
Cabe recalcar que esta ecuación se aplica sólo a semirreacciones y no así para sistemas completos.
Cálculo del potencial de reducción para un sistema en el Punto de Equivalencia (PE)
Para un sistema completo y en equilibrio de la forma
se tiene una constante de equilibrio
y dos ecuaciones de Nernst
En todo momento el sistema se encuentra en equilibrio químico, sin embargo, nos centraremos en el potencial calculado en el punto de equivalencia para lo cual podemos llegar al siguiente modelo para el cálculo del potencial de reducción para un sistema en el PE:
Esta se obtiene igualando los potenciales, se deja la deducción de la misma al lector aunque puedes encontrarla en el Charlot. Para el caso general
La ecuación antes planteada sea adapta como
NOTA: Revisaaaaaaaaar!!!
Su tratamiento puede darse enfocado en el cambio de potencial estándar como del potencial de electrones.
Anfolitos
Cuando en un sistema dado una especie puede actuar como agente oxidante o reductor según sea el caso entonces estamos ante un anfolito, tal es el caso del vanadio pues existe como V2+/ V3+/ V4+ [citar Charlot] donde
Nótese que el actúa como agente oxidante o como reductor según sea el equilibrio a estudiar[3]. Además, el es un polirreductor pues puede recudir tanto al como al .
Podemos estudiar este proceso como una reacción de dismutación si analizamos cómo se descompone el en sus formas oxidada y reducida
Cuan cuantitativa o no sea la dismutación depende las características fisicoquímicas del sistema. Aunque nos centraremos en su contraparte
De forma general
Para calcular el potencial de una disolución de anfolito[3] hacemos uso de la fórmula
Relaciones cuantitativas
Enfoque en el potencial de electrones
Aquí es necesario plantear un equilibrio considerando una concentración de electrones. Para una reacción de la forma:
Planteamos la constante de equilibrio y luego despejamos a la concentración de electrones [e-] para aplicarle el cologaritmo correspondiente. Así obtenemos un potencial de electrón pe- de tal manera que...
Al hacer esto le estamos dando un tratamiento termodinámico. Ahora tenemos que representarlo en el DUZP.
La relación entre el potencial de electrones y el estándar de reducción viene dada por la ecuación:
Enfoque en el potencial estándar de reducción
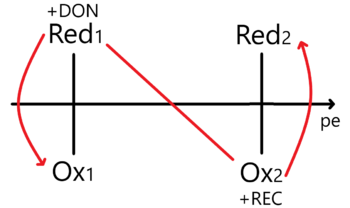
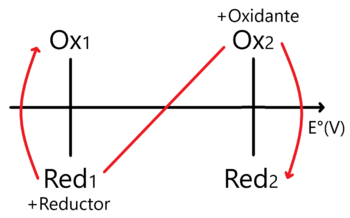
En este caso la regla de la N vista para sistemas Ácido - Base (posible link) se invierte en comparación a como la usamos en Ácidos y Bases.
Nótese que en este caso ubicamos al Oxidante más fuerte en la parte superior derecha y al Reductor más fuerte en la inferior izquierda. En este sentido encontraremos el Proceso Espontáneo y cuya constante de equilibrio se encuentra como:
Donde hemos de sustituir n1 y n2 como los electrones intercambiados por semirreacción involucrada.
Sólo en caso de que sustituimos a uno sólo de estos.
Ejemplos y ejercicios - Equilibrios óxido-reducción
A continuación encontrarás una serie de ejemplos y ejercicios explicados paso a paso para que puedas estudiarlos :)
- Análisis de la variación de potencial de reducción para una titulación de hierro con dicromato
- Gráfico de variación de concentraciones respecto al avance de reacción para la titulación de una solución de estaño con permanganato
- ↑ 1,0 1,1 1,2 Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.
- ↑ Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.
- ↑ 3,0 3,1 Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.