Equilibrios de Óxido-Reducción
Introducción
Visto desde un modelo de intercambio de partícula, las reacciones de óxido-reducción son aquellas en las que ocurre un intercambio electrónico entre un agente oxidante capaz de fijar o recibir electrones (Receptor) de un agente reductor que es capaz de cederlos (Donador)[1] siendo esta una interacción entre donadores y receptores de electrones e- como las partículas a intercambiar, esta reacción química suele representarse de la siguiente manera:
Ox + ne- ⇌ Red
Donde Ox se refiere a la especie Oxidante y Red a la Reductora.
Por ejemplo, podemos considerar al par Fe3+/Fe2+:
Fe3+ + e- ⇌ Fe2+ Donde el Fe3+ fija un electrón e- proveniente del Fe2+, entonces el Fe3+ se reduce (disminuye su estado de oxidación) y en consecuencia permite la oxidación de su contraparte por lo tanto es un agente Oxidante[1]. De la misma manera el Fe2+ se oxida (aumenta su estado de oxidación) permitiendo así la reducción de su contraparte por lo tanto es un agente Reductor[1].
Esto es una semirreacción de óxido-reducción y para completarla necesitamos de una semirreacción más pues los electrones no "viajan" libremente en la disolución (ni siquiera en el cableado eléctrico). Dadas dos semirreacciones estas se suman entre sí anulando la concentración de electrones brindándonos de una reacción completa de óxido-reducción:
Ox1 + ne- ⇌ Red1
Red2 ⇌ Ox2 + ne-
_____________________
Ox1 + Red2 ⇌ Red1 + Ox2
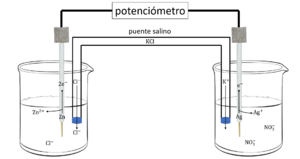
Este tipo de procesos resultan más realistas y hasta reproducibles en laboratorio, por ejemplo en los electrodos de una celda electroquímica tenemos que el proceso de oxidación se lleva a cabo en el ánodo mientras que el reducción en el cátodo de una celda electroquímica.
Ánodo → Ox1 + ne- ⇌ Red1
Cátodo → Red2 ⇌ Ox2 + ne-
______________________________
Celda → Ox1 + Red2 ⇌ Red1 + Ox2
Por ejemplo, en la celda que se muestra podemos apreciar dos pares óxido-reductores. Más adelante revisaremos ejemplos y ejercicios con este tipo de celdas.
Cabe aclarar que esta no es la única definición que existe para una reacción de óxido-reducción, por ejemplo, también podemos considerar a una reacción de este tipo a aquella en la cual tiene lugar un cambio relativo en el orden de las electronegatividades atómicas, entre un átomo dado en uno de los reaccionantes y los átomos con los cuales se encuentra unido antes y después de la reacción; por otro lato y al mismo tiempo, ocurre un cambio similar pero de sentido opuesto en otro de los reaccionantes. La diferencia de las electronegatividades relativas de los átomos que sufren el cambio en el estado de oxidación es un factor determinante en el cambio que sucede[2]. Es importante aclarar que existen más definiciones para este tipo de reacciones pues existen casos particulares que desafían nuestra concepción de reacción de óxido-reducción, tal es el caso de la combustión del carbono C(s) + O2(g) ⮀ CO2(g) ya que no hay realmente un intercambio electrónico debido al enlace covalente C-O. Por ahora nos centraremos en casos más generales que sí implican explícitamente estos intercambios electrónicos.
Ecuación de Nernst
Según la IUPAC el potencial estándar Eo de electrodo es "el valor estándar de la fuerza electromotriz de una celda en la cual el hidrógeno molecular bajo presión estándar es oxidado a protones solvatados en el electrodo de la izquierda"[2][3]. Cada par óxido-reductor tiene asociado un potencial estándar Eo de electrodo normalmente reportado en la literatura, se dicen estándar porque se miden respecto al electrodo estándar de hidrógeno (ESH) al cual le asignamos un potencial de 0.000 V[2] a todas las temperaturas como punto de referencia. En el AMyD de la Facultad de Química, UNAM, podemos encontrar una tabla de potenciales estándar de reducción.
En una celda electroquímica para poder predecir qué reacción se lleva a cabo en cada electrodo es necesario conocer la fuerza de cada par oxidante-reductor siendo que en este caso Ox1 oxida a Red2 ya que Ox2 no puede oxidar a Red1; se dice entonces que Ox1 es un oxidante más fuerte que Ox2 al mismo tiempo que Red2 es un reductor más fuerte que Red1[1].
Para realizar tales predicciones de manera cuantitativa medimos Eo para lo cual suponemos un sistema de dos semirreacciones (una de ellas de 0.000 V pues es ESH y la otra a estudiar) enlazadas mediante un hilo conector inerte (generalmente de platino). Si medimos el potencial eléctrico de equilibrio estaremos midiendo el de la semirreacción de interés y está dado por la Ecuación de Nernst completa cuya forma es:
Donde
- Eo se refiere al potencial estándar de reducción [V] = volts
- R se refiere a la constante de los gases ideales [8.31446 J / mol*K]
- T se refiere a la temperatura absoluta del sistema [K] = Kelvin
- n se refiere a la mol de electrones intercambiados por semirreacción [mol] = NA
- F se refiere a la constante de Faraday [e*NA = 96485.33212 C/mol]
- [Ox] y [Red] refieren a la concentración molar de cada especie oxidante y reductora [mol / L]
Si consideramos a [Ox] = aOx y [Red] = aRed, esto es que la concentración de los agentes es muy similar a sus respectivas actividades termodinámicas.
Si trabajamos en condiciones normales de temperatura (20 °C) y transformando el logaritmo natural a uno base diez podemos aproximar a la ecuación de Nernst simplificada:
Nótese que la constante RT / F se ha simplificado a 0.06 aunque puede usarse 0.0592[2] si se desea todavía más precisión.
En caso de que el sistema esté representado por aOx + ne- ⇌ bRed, entonces la ecuación se adapta como:
Cabe recalcar que esta ecuación se aplica sustituyendo los datos de cada semirreacción y no del sistemas completo. Esta ecuación nos permite calcular el potencial para una disolución que contiene únicamente al par óxido-reducción conjugado[2], nótese que si el sistema se encuentra en equilibrio entonces [Ox] = [Red] y entonces el logaritmo se cancela concluyendo en E = Eo. Fuera del equilibrio si [Ox] > [Red] entonces E > Eo y viceversa, este sistema evoluciona hasta finalmente alcanzar el equilibrio.
Cálculo del potencial de reducción para un sistema en el Punto de Equivalencia (PE)
Para un sistema completo y en equilibrio de la forma
Ox1 + Red2 ⇌ Ox2 + Red1
se tiene una constante de equilibrio
y dos ecuaciones de Nernst
En todo momento el sistema se encuentra en equilibrio químico, sin embargo, nos centraremos en el potencial calculado en el punto de equivalencia para lo cual podemos llegar al siguiente modelo para el cálculo del potencial de reducción para un sistema en el PE:
Esta se obtiene igualando los potenciales, se deja la deducción de la misma al lector aunque puedes encontrarla en el Charlot.
Para el caso general n2Ox1 + n1Red2 ⇌ n1Ox2 + n2Red1 la ecuación antes planteada sea adapta y simplifica como:
Su tratamiento puede darse enfocado en el cambio de potencial estándar como del potencial de electrones.
Anfolitos
Cuando en un sistema dado una especie puede actuar como agente oxidante o reductor según sea el caso entonces estamos ante un anfolito, así sea el sistema:
A + e- ⇌ B
B + e- ⇌ C
Nótese que la especie B actúa tanto como agente oxidante como reductora y por lo tanto es un anfolito. Además C es un polirreductor pues puede reducir tanto a B como a A.
Puesto que los anfolitos son a la vez agentes oxidantes como reductores pueden reaccionar consigo mismos dando lugar a una reacción de dismutación o desproporcionación que, de manera general, se expresa como:
2B ⇌ A + C
Tal es el caso del vanadio[1] pues existe como V2+/ V3+/ V4+ donde:
V4+ + e- ⇌ V3+
V3+ + e- ⇌ V2+
Cuya reacción de dismutación es:
2V3+ ⇌ V2+ + V4+
Aunque nos centraremos en el proceso inverso el cual es una reacción de anfolización, o sea aquella en la formación del anfolito:
A + C ⇌ 2B
V2+ + V4+ ⇌ 2V3+
Cuan cuantitativa o no sea la dismutación o la anfolización depende de las constantes de equilibrio[2]. De forma general para una anfolización:
n2Ox1 + n1Red2 ⇌ (n1 + n2)A
Para calcular el potencial de una disolución de anfolito[1] hacemos uso de la fórmula
Agua
El agua también es un anfolito cuyas semirreacciones son muy variadas según el medio en el que se realizan[2]:
- Como oxidante:
- Medio neutro o alcalino: 2 H2O + 2e- ⇌ H2 + 2 OH-
- Medio ácido: 2 H+ + 2e- ⇌ H2
- Como reductor:
- Medio alcalino: 4 OH- ⇌ O2 + 2 H2O + 4e-
- Medio neutro o ácido: 2 H2O ⇌ O2 + 4 H+ + 4e-
Su comportamiento como agente oxidante o reductor dependen tanto de la especie a la que se enfrente (adquiriendo el carácter opuesto a ella) así como del carácter ácido-base del medio por lo cual es importante entender que el agua no sólo es el medio en el se lleva a cabo el sistema sino que participa activamente en el mismo aunque sus interacciones óxido-reductoras puedan ser débiles o lentas salvo algunas excepciones.
Ejemplos y ejercicios - Equilibrios óxido-reducción
A continuación encontrarás una serie de ejemplos y ejercicios explicados paso a paso para que puedas estudiarlos :)
- Cálculo del potencial para disoluciones que contienen diferentes concentraciones del par conjugado Fe3+/ Fe2+ (Sandoval Márquez, 2011)
- Cálculo del potencial de una disolución con 0.1 mol de Fe2+ y 0.1 mol de Cr3+ por litro (Sandoval Márquez, 2011)
- Cálculo del potencial de una disolución con 0.1 mol de Sn2+ y 0.1 mol de Ce4+ por litro (Sandoval Márquez, 2011)
- Análisis de la variación de potencial de reducción para una titulación de hierro con dicromato
- Gráfico de variación de concentraciones respecto al avance de reacción para la titulación de una solución de estaño con permanganato
Referencias
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Charlot, G. Química Analítica General, Tomo 1, New York, NY, Ed. Toray-Masson, New York, NY, 1980.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Sandoval Márquez, R. (2011). Equilibrios en disolución en química analítica.: Teoría, ejemplos y ejercicios (2.a ed.). Coordinación de Comunicación de la Facultad de Química.
- ↑ 'standard electrode potential' in IUPAC Compendium of Chemical Terminology, 5th ed. International Union of Pure and Applied Chemistry; 2025. Online version 5.0.0, 2025. https://doi.org/10.1351/goldbook.S05912
![{\displaystyle E=E^{o}+{\frac {RT}{nF}}\ln {\frac {[{\text{Ox}}]}{[{\text{Red}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4d47d994e04083b486568334698b8b0c588ac9db)
![{\displaystyle E=E^{o}+{\frac {0.06}{n}}\log _{10}{\frac {[{\text{Ox}}]}{[{\text{Red}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ab39b847e1f207b9e7ef242ae2f4565c38d6a03d)
![{\displaystyle E=E^{o}+{\frac {0.06}{n}}\log _{10}{\frac {[{\text{Ox}}]^{a}}{[{\text{Red}}]^{b}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/19b9c04e6c4ab8704378388a4f486ae440df2b01)
![{\displaystyle K={\frac {[{\text{Red}}_{1}][{\text{Ox}}_{2}]}{[{\text{Ox}}_{1}][{\text{Red}}_{2}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d83bf2f7ae014083c023d4ca9e0f4d585094e258)
![{\displaystyle E=E_{1}+{\frac {0.06}{n}}\log _{10}{\frac {[{\text{Ox}}_{1}]}{[{\text{Red}}_{1}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d0d07ef6cf756edd1bd7f25f0f45a3bf8f0f292f)
![{\displaystyle E=E_{2}+{\frac {0.06}{n}}\log _{10}{\frac {[{\text{Ox}}_{2}]}{[{\text{Red}}_{2}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/45a186f38b00b69cc4228e5345d89f37904433ba)
![{\displaystyle E_{1}-E_{2}={\frac {0.06}{n}}\log _{10}{\frac {[{\text{Ox}}_{2}][{\text{Red}}_{1}]}{[{\text{Red}}_{2}][{\text{Ox}}_{1}]}}={\frac {0.06}{n}}\log _{10}{K}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1347e355422bc92843cf231855498bfc1e4016c8)
![{\displaystyle E={\frac {n_{1}E_{1}^{o}+n_{2}E_{2}^{o}}{n_{1}+n_{2}}}+{\frac {0.06}{n_{1}+n_{2}}}\log _{10}{\frac {[{\text{Ox}}_{1}][{\text{Ox}}_{2}]}{[{\text{Red}}_{1}][{\text{Red}}_{2}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a057a16db532c21d14a882319725b241c3b35c89)

