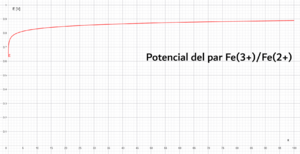
Cálculo del potencial para disoluciones que contienen diferentes concentraciones del par conjugado Fe3+/ Fe2+
Ejemplo recuperado del libro Equilibrios en disolución en química analítica. Teoría, ejemplos y ejercicios de Rebeca Sandoval.[1]
El objetivo de este ejercicio es plantear la función para el cálculo y el gráfico del potencial para disoluciones que contienen diferentes concentraciones del par conjugado Fe3+/Fe2+. Para resolver este problema primero habremos de buscar en la bibliografía a la o las reacciones de óxido-reducción involucradas, según la tabla de potenciales estándar de reducción que se encuentra en el AMyD de la facultad la reacción y su potencial al equilibrio es:
- n = 1, o sea que sólo se intercambia un sólo electrón e-
- Eo = +0.771 V esto es el potencial estándar de reducción para el par redox
- Fe3+ es el agente oxidante
- Fe2+ es el agente reductor
- Nótese que la estequiometría Fe3+:Fe2+ es 1:1
Para el cálculo del potencial haremos uso de la ecuación de Nernst la cual es función de la relación o cociente entre las concentraciones de los agentes oxidante y reductor a lo cual denominaremos como la variable x y esta la graficaremos en el intervalo .
Nótese que no graficamos la función cuando x = 0, ¿Por qué? Porque el logaritmo no queda definido a este valor de x dado que tiende a -∞, a continuación te mostraré el fundamento químico de este y otros límites:
- Cuando el logaritmo tiende a -∞ esto sucede cuando sólo se tiene al agente reductor ([Fe2+]) en solución lo que significa que este "se vuelve infinitamente más fuerte"[2] aunque, en estos casos límite, incluso el medio acuoso participa como la contraparte oxidante así que el potencial no es, explícitamente, infinitamente negativo sino que tiende a valores infinitesimalmente pequeños.
- Cuando el logaritmo tiende a +∞ esto sucede cuando sólo se tiene al agente oxidante ([Fe3+]) en solución, de manera análoga al caso anterior el potencial es indefinidamente grande pues el agua del medio interviene.
Regresar a Equilibrios de Óxido-Reducción.
- ↑ Sandoval Márquez, R. (2011). Equilibrios en disolución en química analítica.: Teoría, ejemplos y ejercicios (2.a ed.). Coordinación de Comunicación de la Facultad de Química.
- ↑ Sandoval Márquez, R. (2011). Equilibrios en disolución en química analítica.: Teoría, ejemplos y ejercicios (2.a ed.). Coordinación de Comunicación de la Facultad de Química.


![{\displaystyle E=+0.771+{\frac {0.0592}{1}}\log _{10}{\frac {[{\text{Fe}}^{3+}]}{[{\text{Fe}}^{2+}]}}=+0.771+0.0592\log _{10}{x}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c4bac01b904ad120a6c1e23ddc58bf814f6f67ed)